胃癌的手术成功率是多少
胃瘟手术成功率是不一定的,但是通常情况下胃癌的手术治疗成功率大多数是在70%~90%左右的,主要是决定于具体患病的严重程度。胃癌手术目的是切除病灶,重建消化道,切除病灶的过程当中与病人病灶发展的程度有密切关系,因为许多胃癌病人发现的时候就是晚期,病灶与周围器官、组织有明显粘连,进行手术切除时,成功率必然下降。
胃癌手术治疗现状
过去70多年里,胃癌发病率在西方国家已逐渐下降,但仍然是世界上最重要的恶性肿瘤之一,发病率和死亡率分别位于第4位和第2位[1]。多数病例在确诊时已属中晚期, 5年生存率为20%-30%[2]。手术切除是目前胃癌的最主要治疗手段,也是唯一可根治的方法[3]。基于此,本文就可切除胃癌的治疗策略进行综述。
首先我们需要先明确手术方式的选择[4],迄今为止,外科手术是治疗胃癌最有效和肯定的方法,和其它癌肿一样,手术应遵循根治性、安全性和有效性三项顺序的原则,落实治疗方法要个体化[5]。
一方面,估计病人能耐受大手术时,尽可能做根治性手术。相当多病人入院时情况较差,但经过充分的术前准备和营养支持,仍有可能行根治性手术。
另一方面,不要过分强调根治术或扩大根治术,对手术耐受差、合并症多、病期晚的病人,充分考虑负荷和耐力,强调手术方式的个体化。
对局限性癌、未侵出浆膜面的浸润型癌或癌肿范围不超过胃的分区,无第3淋巴结转移者,尽可能行根治术[6]。
对病变范围较大、超过胃分区的胃体癌作全胃切除,胃底贲门癌实行近端胃大部切除术。
Ⅳ期且有腹膜转移、肝转移、远处淋巴结转移者,尽可能切除原发病变(胃大部切除),减轻机体的免疫负荷,改变机体与肿瘤的比势,为以后的综合治疗创造条件。
改善病人的生存质量,对有幽门梗阻而病变又不能切除者,可行胃肠吻合。在基层医院中,术者层次差异很大,亲自能做胃镜检查者不多,用多种手段(如钡餐、CT、癌标等)检查,作为术前病理类型与TNM估计者更少,术中探查基本是胃外观察,门诊对肿瘤位置大小、浆膜表现、胃周淋巴结与组织(器官)受累情况描述粗疏。
由此造成切除范围不够、遗留多发癌灶、放弃巨大局限生长型肿瘤等遗憾[7]。现代肿瘤学强调,肿瘤外科医生必须在肿瘤生物学的基础上作出治疗决策,即除对病人的全身情况全面了解外,着重对原发癌灶及其局部扩散的准确判断,包括癌肿的类型、分级、TNM分期,从而为选择适合病人的最佳手术方案提供保证[8]。
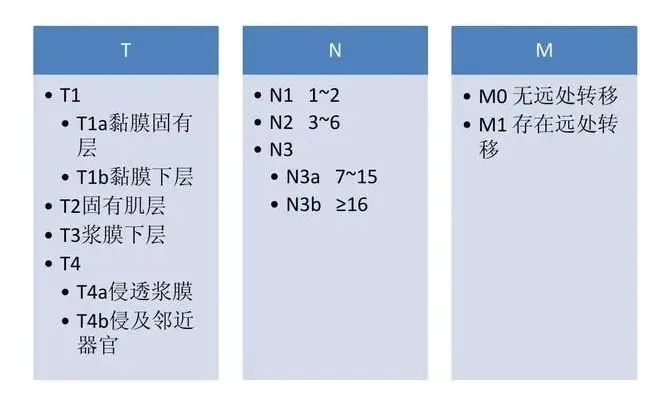
图片源自网络
根据传统的胃癌切除方法,D以上的手术,必须采用全麻,切口采用自剑突至脐下5cm中线直切口或上腹部斗蓬式切口。要用自动开腹钩或悬吊式拉钩上提肋弓,以保证术野宽广。
后腹膜重要血管的全程暴露,多数情况下,先行Kocker切口游离切断十二指肠→大小网膜,胰包膜→将胃提向左上方,切断胃脾韧带→显露左胃血管镰→切开裂孔腹膜并游离食道下端[9]。
个别情况,用电刀与双极电凝沿肝门、胰头后、肝动脉、胃左血管根部三结构、结肠中血管、肠系膜上血管、腹主动脉,循序将相关淋巴结及其周围脂肪结缔组织予以分段或整块切除。
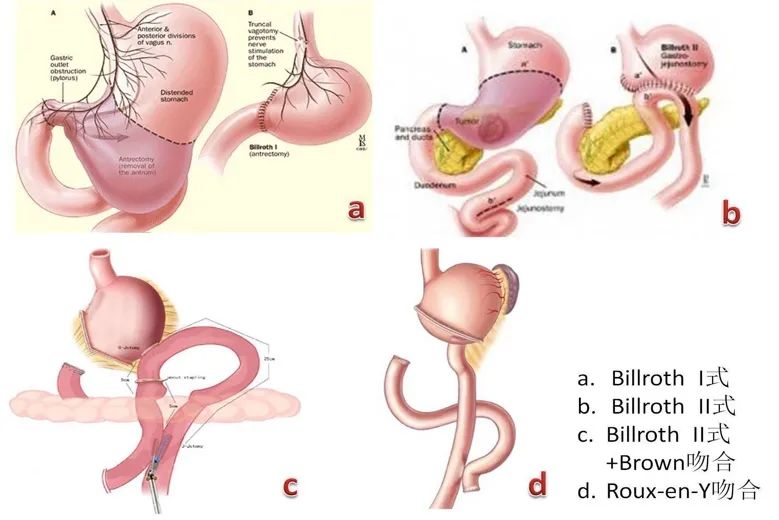
图片源自网络
术后的综合治疗同样重要,这是因为胃癌术后复发的治疗颇为棘手,若能早期发现癌肿复发,再次施行根治性手术往往可获得较满意疗效。
胃癌复发后二次手术的类型
目前胃癌术后复发的再手术治疗通常包括三大类手术,即根治性切除术、转移复发灶切除术和姑息性手术。
根治性切除术,其指征主要为残胃内或胃肠吻合口癌肿复发,并已排除远处转移者,手术方式为根治性全胃切除,包括淋巴结扩大清扫,必要时可联合脾脏和胰腺体尾切除,以彻底廓清转移之淋巴结。
据文献报告,若复发癌灶局限并能再获根治性切除者,5年生存率仍可达到30%以上[10]。
转移复发灶切除术,主要针对某一脏器或腹膜单个或局限性复发灶的切除,根据肝脏的转移复发程度,应施行不同的外科治疗对策,对于局限于肝脏一叶内或单灶性转移复发灶,可行肝叶切除术或转移复发灶切除。
以此达到的中位生存期为12-21个月不等,5年生存率仍达18%-38%[11]。而对已累及左右两叶的多发性转移复发灶,则通常以经肝动脉介入治疗为首选。
对于局限性的腹膜转移灶,近年来也提出了部分腹膜切除术辅以腹腔内温热化疗等综合治疗措施。
根据腹膜转移复发的部位,可分别施行某一区域的腹膜切除术,例如右上腹腹膜切除术、左上腹腹膜切除术、盆腔腹膜切除术等。
术者应尽量切除腹膜表面的复发癌灶,使之残留的肿瘤越少,腹腔内化疗的效果亦越好[12]。
姑息性手术,该类手术主要是以缓解临床症状或达到去肿瘤负荷为目的,旨在减轻恶液质,减少并发症,延长生命,并为配合其它综合治疗创造条件。
胃癌术后复发的化疗为综合治疗最主要的手段,所有癌肿复发的病人均应给予积极的化疗,化疗途径包括全身性和区域性两大类,随着一些高效低毒化疗新药的问世以及新辅助化疗在临床的普及应用,全身性化疗的疗效已有较大改善。
目前对胃癌新辅助化疗如何选择疗效更好、更安全的化疗方案已成为国内外学者近年研究的热点[13]。近年来多西他赛联合5-FU、顺铂治疗胃癌的报道较多。
多西他赛是半合成紫杉类抗肿瘤药物,主要通过促进肿瘤细胞内微管聚合及抑制微管蛋白解聚,使游离微管的数量减少,抑制肿瘤细胞的有丝分裂,从而导致肿瘤细胞死亡。
有研究报道其单药应用的有效率为17%~24%。顺铂属细胞周期非特异性药物,与多西他赛联合应用可产生协同作用,且可减少顺铂的用量。
且大量的临床经验表明[14],患者术前新辅助化疗的耐受性显著强于术后辅助化疗,新辅助化疗疾病控制率高, 原发灶与转移灶均可获得不同程度的缓解,一般化疗2~4个周期即可达到疗效最大化。
综上所述,可切除胃癌的临床治疗观念和水平仍有待进一步提高。胃癌的分期是决定其预后的重要因素,分期偏低的胃癌有可能通过扩大根治方案获得治愈,分期偏高的病例不应奢望通过扩大手术方案以寻求根治,应争取采用以手术为主的临床综合性治疗,以期能延长患者的术后远期生存期。
参考文献:
[1] PARKIN D M, BRAY F, FERLAY J, et al. Global cancer statistics, 2002 [J]. CA: A cancer journal for clinicians, 2005, (2): 55.
[2] 朱正纲. 早期胃癌的临床病理特征及其外科治疗 [J]. 中国医师杂志, 2003, 5(002): 145-7.
[3] 杨林, 王金万, 陈平. 可切除胃癌术后辅助化疗现状 [J]. 癌症进展, 2005, (1): 4.
[4] 刘洪伟, 楚海成. 可切除进展期胃癌治疗策略与措施的探讨 [J]. 当代医学, 2008, 25(003): 314-7.
[5] 陈峻青. 胃癌外科治疗的现状与未来 [J]. 中国实用外科杂志, 1999, 19(1): 2.
[6] 王舒宝. 复发胃癌及晚期胃癌的外科治疗 [J]. 中国实用外科杂志, 2000, 20(10): 2.
[7] 张延龄. 实用外科学 [M]. 实用外科学, 2012.
[8] 吴功侃, 赵荣宇. 提高可切除进展期胃癌疗效的策略与措施 [J]. 中国实用外科杂志, 1998, 18(8): 3.
[9] KIKUCHI S, KATADA N, SAKURAMOTO S, et al. Factors Associated with pN3 Stage Tumors According to the TNM Classification in Advanced Gastric Cancer [J]. HEPATOGASTROENTEROLOGY, 2003.
[10] KITANO S, SHIRAISHI N, UYAMA I, et al. A multicenter study on oncologic outcome of laparoscopic gastrectomy for early cancer in Japan [J]. Annals of surgery, 2007, 245(1): 68.
[11] 彭淑牖. 晚期胃癌不要轻易放弃手术切除的机会 [J]. 中国实用外科杂志, 2001.
[12] 尹浩然, 朱正纲, 林言箴. 进展期胃癌外科综合治疗的方法与步骤 [J]. 外科理论与实践, 2000, 5(3): 2.
[13] VITA F D, GIULIANI F, GALIZIA G, et al. Neo-adjuvant and adjuvant chemotherapy of gastric cancer - ScienceDirect [J]. Annals of Oncology, 2007, 18.
[14] 杨熙华, 金钦文, 王力, et al. 潜在可切除胃癌新辅助化疗的临床疗效观察 [J]. 中国癌症防治杂志, 2013, 5(4): 324-7.
内容来源:领募圈
